De beoordeling van biologische risico's is een proces dat bestaat uit de identificatie van mogelijke negatieve gevolgen voor de menselijke gezondheid of het leefmilieu ten gevolge van een bepaald gebruik van een GGO of pathogeen, de waarschijnlijkheid dat die gevolgen zich voordoen en de ernst ervan. Een bewezen risico leidt tot de toepassing van geschikte preventiemaatregelen.
Op deze pagina
- Inleiding
- Uitvoeren van de risicobeoordeling
- Voorzorgsbeginsel
- Activiteit van ingeperkt gebruik
- Doelbewuste introductie
- Internationaal erkende methode
- Controverse
Inleiding
De beoordeling van biologische risico's berust niet op een door technocraten ontwikkelde theoretische grondslag, maar wel op een empirische grondslag naar aanleiding van een zekere bewustwording bij de wetenschappelijke gemeenschap van enerzijds het gevaar van de manipulatie van pathogene organismen (ten gevolge van inventariseringen van in laboratoria verworven infectieziekten) en anderzijds het mogelijke gevaar van manipulaties met recombinant-DNA.
Die beoordeling vormt de wetenschappelijke grond om elke activiteit met GGO's en/of pathogenen toe te staan dan wel te verbieden en om eventueel maatregelen op te leggen om de potentiële risico's voor de menselijke gezondheid en het leefmilieu te beperken.
Risicobeoordeling is één van de drie elementen van een risicoanalyse de twee andere zijn het risicobeheer (dat traditioneel tot de taak van de beslissingsbevoegde organen behoort) en de risicocommunicatie (met name ten aanzien van het publiek). In theorie zijn dit drie afzonderlijke en opeenvolgende elementen, maar in de praktijk blijken de grenzen ertussen soms nogal vaag en poreus.
Uitvoeren van de risicobeoordeling
De risico-evaluatie van de activiteiten van ingeperkt gebruik met pathogenen en van de activiteiten met ggo's moeten geval per geval worden uitgevoerd (dat wil zeggen dat het afhankelijk is van het GGO of de desbetreffende pathogeen, de geïntroduceerde genen, en het beoogde gebruik) terwijl wordt ook gebaseerd op gevestigde wetenschap (bekende wetenschappelijke feiten, resultaten gepubliceerd in erkende wetenschappelijke tijdschriften). De introductie van GGO's in het milieu dient stapsgewijs plaats te vinden; dit houdt in dat de inperking van de GGO's geleidelijk en stapsgewijs wordt verminderd en de schaal waarop de introductie plaatsvindt, geleidelijk en stapsgewijs wordt vergroot, doch alleen indien uit de beoordeling van de eerdere stappen met betrekking tot de bescherming van de menselijke gezondheid en het milieu blijkt dat de volgende stap kan worden gezet. De beoordeling toegepast op elke verdere stap houdt dus rekening met de resultaten verkregen tijdens de vorige stappen.
In overeenstemming met de bovenstaande beginselen en methode, moet een beoordeling van biologisch risico in zes stappen worden uitgevoerd, in een geïntegreerd proces en op een iteratieve wijze, als volgt :
- De bepaling van de kenmerken van de GGO of pathogeen die schadelijke effecten (gevaar) op de gezondheid van de mens of op het milieu kunnen veroorzaken, van de aard van deze effecten en van de blootstellingsroutes via dewelke het GGO of pathogeen een negatieve invloed kan hebben op de gezondheid van de mens of op het milieu. In geval van een milieurisicobeoordeling (doelbewuste introductie van GGO's) is deze eerste stap ontworpen binnen een "probleemstelling", een proces waarbij alle belangrijke vragen voor de risicoskarakterisering worden geïdentificeerd;
- Karakterisering van het gevaar namelijk de beoordeling van de mogelijk gevolgen van elk schadelijk effect;
- Karakterisering van de blootstelling namelijk de beoordeling van de waarschijnlijkheid van het optreden van elk mogelijk schadelijk effect;
- Karakterisering van de risico's namelijk de inschatting van het risico verbonden aan elk bepaalde kenmerk van het GGO of pathogeen die potentieel schadelijke effecten kunnen veroorzaken;
- Toepassing van risicobeheersmaatregelen om potentieel geïdentificeerde risico's verbonden aan het GGO of de pathogeen, tot een verwaarloosbaar niveau te verlagen, en om de onzekerheden aan te pakken;
- Bepaling van het algemene risico van de GGO of pathogeen, rekening houdend met de resultaten van de risicobeoordeling en de bijbehorende niveaus van onzekerheid en de voorgestelde risicobeheersmaatregelen.
Tot dusver werden wereldwijd tal van risicobeoordelingen uitgevoerd voor zowel het ingeperkt gebruik van GGO's of pathogenen als de doelbewuste introductie van GGO's in het leefmilieu of hun gebruik als levensmiddel, diervoeder of geneesmiddel. De basis van die risicobeoordelingen ontwikkelde zich geleidelijk aan, waarbij rekening werd gehouden met de meest recente wetenschappelijke gegevens en technieken.
Voorzorgsbeginsel
Het is belangkrijk om een onderscheid te maken tussen preventie- (als reactie op een bewezen risico) en voorzorgsmaatregelen. Volgens de Europese Commissie (Mededeling van de Commissie van 2 februari 2000 over het voorzorgsbeginsel) kan het voorzorgsbeginsel worden ingeroepen wanneer er aan de hand van een objectief en wetenschappelijk onderzoek mogelijk gevaarlijke gevolgen van een fenomeen, product of procedé zijn vastgesteld, zonder dat dit onderzoek het risico met voldoende zekerheid kan bepalen. Het beroep op het voorzorgsbeginsel past bijgevolg in het algemene kader van de risicoanalyse, maar valt onder het risicobeheer. Het beroep op het voorzorgsbeginsel is uitsluitend gegrond wanneer aan drie voorafgaande voorwaarden – de identificatie van mogelijk negatieve gevolgen, de beoordeling van beschikbare wetenschappelijke gegevens en de omvang van de wetenschappelijke onzekerheid – is voldaan.
De risicobeoordeling van GGOs en pathogenen houdt geen rekening met verwante voordelen, noch met andere maatschappelijke, economische of ethische aspecten van het gebruik van het beoordeelde organisme. Die aspecten worden eventueel door de risicomanagers in aanmerking genomen op het moment dat zij een besluit nemen. We merken op dat er steeds meer stemmen opgaan op Europees en internationale niveau om de mogelijke sociaal-economische gevolgen van het gebruik van GGO's aan een specifieke beoordeling te onderwerpen, in het bijzonder in het context van hun cultivatie of gebruik als voedingsmiddelen. De vraag of een dergelijke beoordeling in het huidige risicobeoordelingsproces moet worden opgenomen of afzonderlijk moet worden gevoerd, blijft voorlopig onbeantwoord.
Activiteit van ingeperkt gebruik
In het geval van een ingeperkt gebruik leidt die procedure tot de identificatie van het risiconiveau voor het betreffende GGO of pathogeen. Op basis daarvan wordt vervolgens bepaald welke inperkings- en andere beschermingsmaatregelen getroffen moeten worden (werkpraktijken, veiligheidsuitrusting, beheer van biologisch besmettelijk afval). Aan de hand van de uitgevoerde analyse wordt het ingeperkt gebruik in één van de 4 bestaande risicoklassen ingedeeld (risicoschaal van 1 tot 4). De laatste stap bestaat erin het ingeperkt gebruik definitief in te delen, wat door een nieuwe beoordeling van de volledige procedure bevestigd wordt.
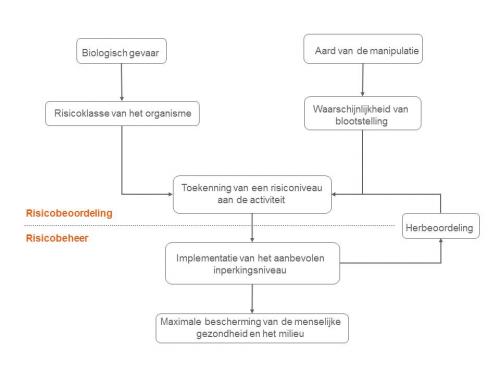
Toepassing van de risicobeoordeling en aanname van risicobeheersmaatregelen in geval van een ingeperkt gebruik van GGO's en/of pathogenen
Doelbewuste introductie
In geval van een doelbewuste introductie in het leefmilieu (voor onderzoeks- of commerciële doeleinden) of van een gebruik voor voedingsdoeleinden, moeten de GGO's volledig gekarakteriseerd worden op moleculair vlak. De aspecten met betrekking tot de eventuele consumptie van GGO's (toxiciteit, allergenisch potentieel, analyse van de samenstelling, voedingswaarde) en/of de milieu-impact ervan (agronomische parameters, mogelijkheid tot introductie of overdracht van genen, impact op niet-doelsoorten ...) worden ook aan een grondige beoordeling onderworpen.
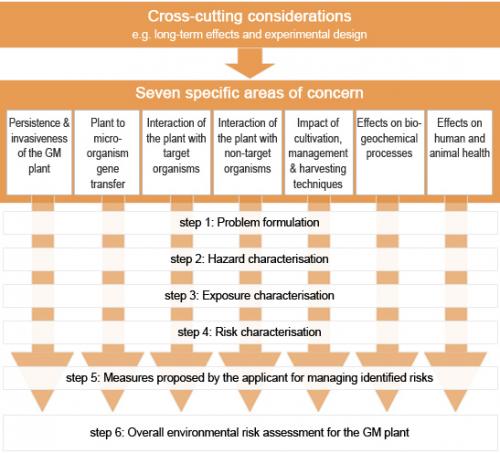
Methodologie voor de milieurisicobeoordeling voor een GG plant (Bron: https://www.efsa.europa.eu/en/topics/topic/gmo)
We merken op dat de milieurisicobeoordeling ook wordt toegepast op GGO's voor medische doeleinden die tijdens een gentherapeutische proef of vaccinatie worden gebruikt of waarvoor een aanvraag is ingediend om in de handel te brengen.
In geval van een doelbewuste introductie, bestaat de risicobeoordeling uit een vergelijkende analyse om de eventuele verschillen te bepalen tussen het GGO en zijn niet genetisch gemodificeerde equivalent, gevolgd door een beoordeling van de nutritionele, gezondheid of milieu-impact van die verschillen. Die vergelijkende aanpak is op twee concepten gebaseerd: het concept van bekendheid en het concept van wezenlijke gelijkwaardigheid.
| Het concept van bekendheid bepaalt dat de risicobeoordeling van een GGO een beroep kan doen op de kennis en ervaring die reeds beschikbaar is met de niet-gemodificeerde gastheer organisme, de nieuwe kenmerk, het ontvangende milieu en de interacties tussen deze (zie ook OECD, 1993). Het impliceert dat de niet-genetisch gemodificeerde organisme die gebruikt wordt om een GGO te ontwikkelen, terecht als vergelijkingselement kan worden gebruikt om de verschillen ten gevolge van de genetische modificatie te kunnen identificeren. De OECD ontwikkelde verschillende standaarden (de zogenaamde "consensus documenten") om de bekendheid te beoordelen. |
| Het concept van wezenlijke gelijkwaardigheid specificeert dat de mogelijke risico's ten gevolge van de verschillen in samenstelling tussen het GGO en zijn niet-GG equivalent moeten worden bestudeerd. Dit begrip wordt eerst in 1993 door de OESO verklaard in het kader van de risicobeoordeling van levensmiddelen uit de moderne biotechnologie. Het wordt nu op internationaal niveau veel gebruikt bij de beoordeling van de gezondheidsrisico's van GGO's voor voedingsdoeleinden (het gebruik in dit kader werd goedgekeurd door de FAO en de WHO). De beoordeling van de wezenlijke gelijkwaardigheid houdt in dat de aanwezigheid en concentratie van een reeks belangrijke bestanddelen van het levensmiddel (proteïnen, vitaminen, koolhydraten, toxines, antinutrients...) worden gemeten. Een GG product wordt wezenlijk gelijkwaardig aan diens niet-GG tegenhanger beschouwd, wanneer diens eigenschappen van samenstelling binnen de normale waarden vallen voor natuurlijke variatie voor de niet-GG referenties. De vaststelling van wezenlijke gelijkwaardigheid is geen gezondheidsrisicobeoordeling op zich, maar een analytisch element en indicatie voor de risicobeoordeling, wat toelaat om een beslissing te nemen omtrent het verder verloop van de beoordeling. Indien verschillen in samenstelling geïdentificeerd werden tussen de GG plant en diens niet-GG tegenhanger, moeten gerichte toxicologische en nutritionele studies uitgevoerd worden om de veiligheid en de impact op de voedingswaarde voor de mens te beoordelen. (Kok and Kuiper, 2003). |
Internationaal erkende methode
De basisprincipes van de beoordeling van biologische risico's zijn voortgevloeid uit diverse werkzaamheden op internationaal niveau, in het bijzonder binnen de OESO (zie ook "Historische achtergrond"). In de loop van de jaren wordt die tendens voortgezet en nog versterkt, zoals bijvoorbeeld blijkt uit de werkzaamheden in het kader van de Codex Alimentarius met betrekking tot de voedingsnormen of in het kader van het Protocol van Cartagena inzake bioveiligheid. In die instanties worden, net als elders, groepen van deskundigen er regelmatig toe aangezet om de methodologie voor de beoordeling van biologische risico's te verfijnen, te preciseren of te illustreren om bijvoorbeeld op nieuwe soorten organismen (insecten, bomen, vissen, virussen ...) of nieuwe kenmerken (bijvoorbeeld weerstand tegen droogte of andere extreme omstandigheden) toe te passen. Hoewel bepaalde aspecten van de beoordeling van biologische risico's meer dan eens in vraag worden gesteld (zoals de toepassing van het begrip wezenlijke gelijkwaardigheid bij de beoordeling van GGO's voor voedingsdoeleinden), blijven de algemene principes tot op vandaag onveranderd.
In de loop van de tijd evolueerde vooral op het vlak van GGO's de wetenschappelijke vertegenwoordiging van deskundigen die bij de beoordeling van biologische risico's betrokken zijn. Terwijl bij het ontstaan van bioveiligheid de moleculaire biologen de boventoon voerden, herbergt de discipline nu ook in milieu gespecialiseerde wetenschappers, voedingsdeskundigen, toxicologen of allergologen.
Controverse
Het grote aantal nuttige wetenschappelijke gegevens en studiegevallen ter ondersteuning van de risicobeoordelingen nam in de loop van de jaren ook aanzienlijk toe. Die ontwikkeling droeg uiteraard bij tot een betere risicobeoordeling. Maar ze doet paradoxaal genoeg ook meer vragen rijzen. Of zoals Di Castri (1992) het al omschreef: "Je moet je de kennis als een bol voorstellen. Naarmate zijn volume groter wordt, neemt het aanrakingsvlak met het onbekende toe." (Di Castri F. L’écologie en temps réel. In Theys J. en Kalaora B., (Dir.) La terre outragée. Les experts sont formels! Ed. Autrement, Paris, 1992.)
Dat de risicobeoordeling nieuwe vragen doet rijzen, is op zich allesbehalve abnormaal, net zoals bovendien het gebrek aan consensus tussen wetenschappers over de interpretatie van bepaalde gegevens. Dat is een natuurlijk gevolg van de wetenschappelijke benadering die niet eenduidig maar tegenstrijdig is. Die vraagstellingen zouden dan ook moeten leiden tot nieuwe onderzoeken en het ontstaan van bijkomende gegevens. Helaas wordt de ontwikkeling van het onderzoek inzake bioveiligheid belemmerd door onder andere financiële problemen, de vernietiging van percelen voor veldproeven op transgene planten, het gebrek aan interesse voor dit soort onderzoek en tal van andere factoren.
De wetenschappelijke controverse voedt ook al te vaak de polemiek in plaats van het wetenschappelijke debat. De voorbije jaren bleek dat zeer duidelijk op het vlak van GGO's. Meerdere factoren liggen aan de oorsprong van die situatie: de bekendmaking aan het grote publiek van preliminaire wetenschappelijke resultaten, de ongegronde veralgemening van wetenschappelijke conclusies, het isoleren van bepaalde proefresultaten uit hun context (de beoordeling van biologische risico's is een incrementeel en holistisch proces waarbij de wetenschappelijke gegevens in hun geheel moeten worden beschouwd) of de verwarring tussen "gevaar" en "risico".
